谈谈美国那“聊胜于无”的免费年检
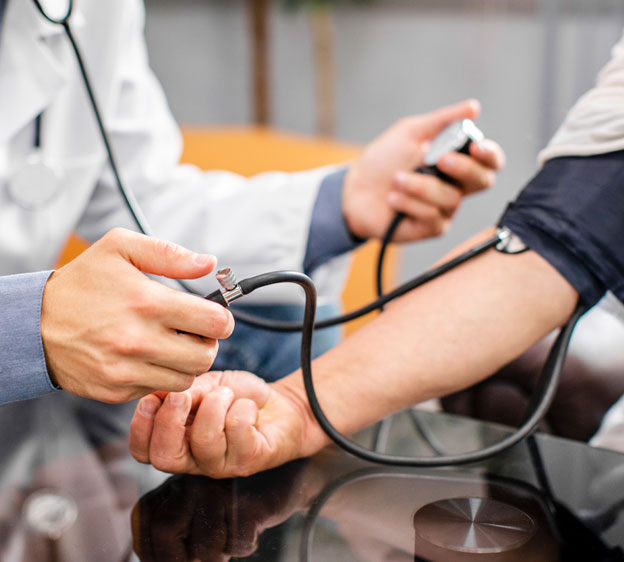
谈谈美国那“聊胜于无”的免费年检 朱自强 刘伟医生 之前讲过国内体检的体检套餐(体检套餐—–想说爱你不容易),接下来聊聊美国医疗保险提供的年检。 体检,顾名思义显然是指身体的常规健康检查。很多人都知道或使用过自己保险公司提供的所谓一年一次的免费体检,总觉得犹如鸡肋–“食之无味、弃之可惜”。 一方面觉得没有国内体检套餐来的“快准狠”—-想查什么就可以查什么。 另一方面,觉得在美国体检很多时候只是和医生聊聊天,最多就是抽个血、验个小便,基本没有提供能够告诉你身体“真实情况”的影像学检查比如X光、超声波、CT或磁共振等,难不成美国的家庭医生都有火眼金睛,不需要这些更加高大上的检查方法吗?答案显然不是的。 由于绝大部分美国人都有医疗保险(联邦政府、州政府提供或是商业的保险等),而且绝大部分保险公司都提供并且鼓励一年一次的免费体检,但事实上“并不是所有的体检都是一样的”。 如果我说,美国有的保险提供年检甚至都不需要医生触碰病人、也不需要抽血检查,完全在谈话之中就完成所谓一年一次的年检,您是不是会觉得相当诧异惊讶呢? 美国的Medicare(红蓝卡)提供一年一次的Annual Wellness Visit (健康体检)。 Medicare医疗保险计划是美国联邦政府为大部分65周岁及以上的老年人,以及小部分65周岁以下的特殊人群(包括残疾人士以及终末期肾病需要透析的患者)提供的医疗保险计划。 加入Medicare的12个月之内,保险计划会建议您找自己的家庭医生做一次Welcome to Medicare的体检,之后每年都建议看家庭医生做一年一次的Annual Wellness Visit。 这个一年一次的Wellness